Cho 26 gam zinc tác dụng với dung dịch có chứa 18,25 gam hydrochloric acid.
a) Tính khối lượng muối tạo thành sau phản ứng.
b) Tính khối lượng dung dịch hydrochloric acid ban đầu biết nồng độ dung dịch là 20%.
c) Dẫn toàn bộ khí sinh ra ở trên đi qua bột iron(II) oxide nung nóng thì có bao nhiêu gam iron (II) oxide bị khử. (Zn=65;H=1;Cl=35,5;Fe=56;O=16)
giúp mình với ạ, mình không biết làm mà mai phải nộp rồi =((
những ai giúp mình thì cho mình gửi lời cảm ơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 9 :
\(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
0,05--->0,1-------->0,05
a) \(C_{MddHCl}=\dfrac{0,1}{0,1}=1\left(M\right)\)
b) \(m_{CuCl2}=0,05.135=6,75\left(g\right)\)
c) \(C_{MCuCl2}=\dfrac{0,05}{0,1}0,5\left(M\right)\)
Câu 10 :
\(n_{FeO}=\dfrac{3,6}{72}=0,05\left(mol\right)\)
\(FeO+2HCl\rightarrow FeCl_2+H_2O\)
0,05-->0,1------->0,05
\(m_{ddHCl}=\dfrac{0,1.36,5}{10\%}100\%=36,5\left(g\right)\)
\(m_{ddspu}=3,6+36,5=40,1\left(g\right)\)
\(C\%_{FeCl2}=\dfrac{0,05.127}{40,1}.100\%=15,84\%\)

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,3\left(mol\right)\\n_{ZnCl_2}=0,15\left(mol\right)=n_{H_2}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\m_{ZnCl_2}=0,15\cdot136=20,4\left(g\right)\\C_{M_{HCl}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)

a, Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
b, \(n_{Fe}=\dfrac{6,5}{65}=0,1mol\\ \Rightarrow n_{HCl}=0,1.2=0,2mol\\ \Rightarrow m_{HCl}=0,2.65=13g\)
c, \(m_{ZnCl_2}=0,1.136=13,6g\)
\(V_{H_2}=0,1.24,79=2,479l\)
a) Chất tham gia phản ứng là : Kẽm ( Zn ) và dung dịch axit clohidric ( HCl )
b) Dấu hiệu để nhận biết có phản ứng hóa học xảy ra : Kẽm ( Zn ) tác dụng với HCl tạo ra chất khác ( ZnCl2)
c) PTHH :
Kẽm + axit clorua --------> kẽm clorua + hidro
d) Theo định luật bảo toàn khối lượng có :
mZn + mHCl = mZnCl2 + mH2
=> 6.5 + mHCl = 13.6 + 0.2
=> mHCl = 13.6 + 0.2 - 6.5 = 7.3 ( g )
Khối lg HCl có trong dung dịch là : 7.3 ( g )
Ủng hộ nhak !!!

\(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,15 0,4 0,15
a) Lập tỉ số so sánh : \(\dfrac{0,15}{1}< \dfrac{0,4}{2}\)
⇒ Zn phản ứng hết , HCl dư
⇒ Tinsht toán dựa vào số mol của zn
\(n_{HCl\left(dư\right)}=0,4-\left(0,15.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
b) \(n_{H2}=\dfrac{0,15.1}{1}=01,5\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,15.24,79=3,1875\left(l\right)\)
Chúc bạn học tốt

Bài 6:
\(n_{Fe\left(OH\right)_3}=\dfrac{21,4}{107}=0,2\left(mol\right)\)
PT: \(Fe\left(OH\right)_3+3HCl\rightarrow FeCl_3+3H_2O\)
_______0,2________0,6______0,2 (mol)
a, \(C\%_{HCl}=\dfrac{0,6.36,5}{200}.100\%=10,95\%\)
b, \(C\%_{FeCl_3}=\dfrac{0,2.162,5}{21,4+200}.100\%\approx14,68\%\)
Bài 7:
\(m_{H_2SO_4}=100.9,8\%=9,8\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PT: \(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
______0,1______0,1_______0,1 (mol)
a, \(m_{ZnO}=0,1.81=8,1\left(g\right)\)
b, \(C\%_{ZnSO_4}=\dfrac{0,1.161}{8,1+100}.100\%\approx14,89\%\)
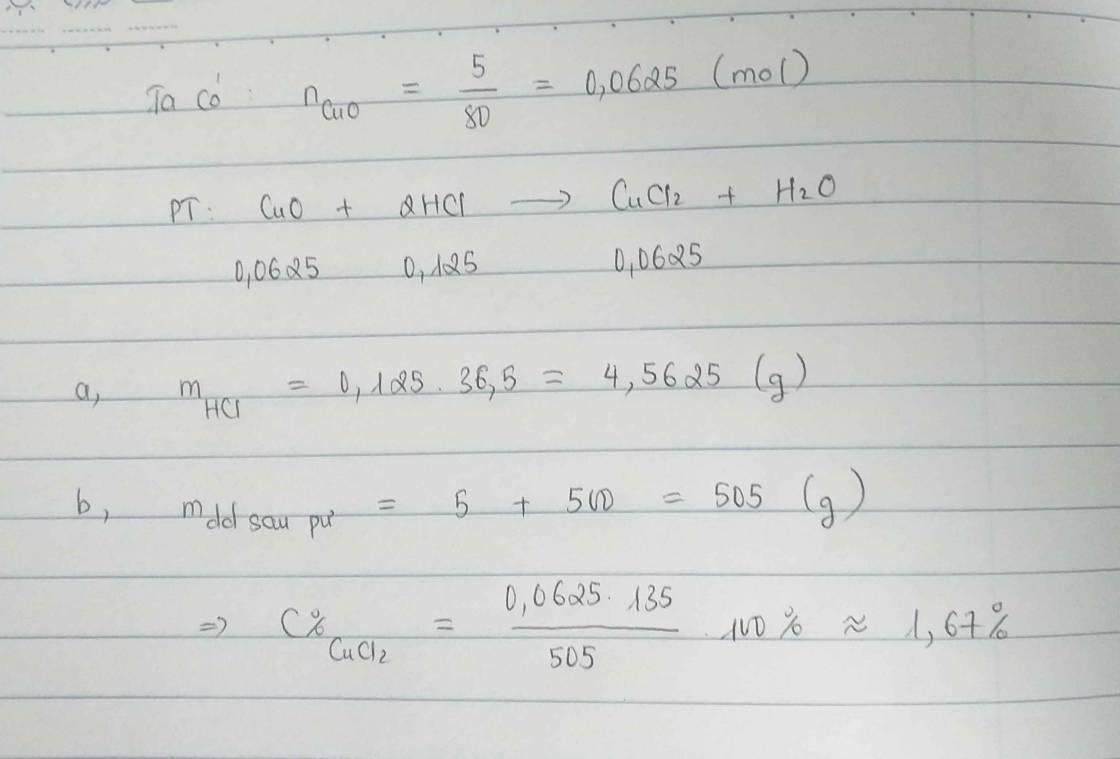
a, \(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,5}{2}\), ta được Zn dư.
Theo PT: \(n_{ZnCl_2}=\dfrac{1}{2}n_{HCl}=0,25\left(mol\right)\Rightarrow m_{ZnCl_2}=0,25.136=34\left(g\right)\)
b, \(m_{ddHCl}=\dfrac{18,25}{20\%}=91,25\left(g\right)\)
c, \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,25\left(mol\right)\)
PT: \(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
Theo PT: \(n_{FeO}=n_{H_2}=0,25\left(mol\right)\Rightarrow m_{FeO}=0,25.72=18\left(g\right)\)