1.Chia hỗn hợp X gồm: ancol etylic và axit axetic (biết số mol ancol nhiều hơn số mol axit) thành 2 phần bằng nhau. Phần 1: cho tác dụng hết với Na dư thu được 5,6 lít (đktc). Phần 2: đun nóng với đặc (Hiệu suất phản ứng este hóa là 50%), thu được 4,4 gam este. Số mol ancol và axit trong hỗn hợp X lần lượt bao nhiêu?
2.Khi đun nóng 25,8 gam hỗn hợp X gồm rượu etylic và axit axetic có H2SO4 đặc làm xúc tác thu được 14,08 gam este. Nếu đốt cháy hoàn toàn lượng hỗn hợp X thu được 23,4g H2O. Hiệu suất của phản ứng este hoá là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án là D
Gọi số mol ancol và acid trong 1 phần X lần lượt là x, y mol ( x>y)
tác dụng với Na ![]() = 0,25
= 0,25
=> x+y= 0,5
este hóa CH3COOC2H5
meste = y.0,5.88=4,4
=> y=0,1 => x=0,4
=> số mol ancol, acid trong X lần lượt là 0, 8 và 0,2 mol

Đáp án A
n ancol, ax = 0,5 => n ancol, ax trong X =1
neste = 0,1
Vì nancol > nax => ancol dư
CH3COOH+C2H5OH→CH3COOC2H5 + H2O
0,1
=> Trong X: nax =0,2; nancol = 0,8

Đáp án B
Chia hh M thành 2 phần bằng nhau nên:
Phần 1 ta được
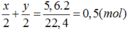
Phần 2 ta được
![]()
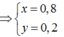

Đáp án A
nH2 = 0,055 mol
Giả sử số mol của CH3COOH và C2H5OH trong 11,52 gam lần lượt là x, y
Ta có hpt:
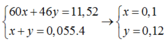
• 0,05 mol CH3COOH và 0,06 mol C2H5OH đun với H2SO4 đặc. H = 80%.
CH3COOH + C2H5OH <=> CH3COOC2H5 + H2O
→ m = 0,05 x 88 x 80% = 3,52 gam → Chọn A.

Đáp án D
Phần 2:
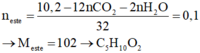
Gọi số C trong axit là a, trong ancol là b
Do số mol của axit nhỏ hơn ancol nên → nancol – naxit = 0,1 mol
Mặt khác,

Như vậy, sau phản ứng ancol dư 0,1
Số CO2 chênh lệch giữa 2 phần chính là CO2 do ancol dư tạo ra
Số C trong ancol:
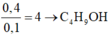
Như vậy, số C trong axit:
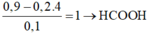

Đáp án D
Xét phần 2:
C n C O 2 = n H 2 O = 0 , 5 ( m o l ) ; m e s t e = m C + m H + m O = 12 n C O 2 + 2 n H 2 O + 16 n O t r o n g e s t e ⇒ n O t r o n g e s t e = 0 , 2 ( m o l )
Vì este đơn chức =>neste = 0,1 (mol)
=>este có 5 nguyên tử C trong phân tử
=> công thức este là C5H10O2 (1)
Xét phần 1 ta có:
n a x i t = n a n c o l = 0 , 3 ( m o l ) ; n C O 2 = 0 , 9 ( m o l ) ⇒ C ¯ a x i t v à a n c o l = 3 ( 2 )
Từ (1) và (2) suy ra trong axit và ancol, 1 chất có 1 nguyên tử C, 1 chất có 4 nguyên tử C
Lại có: naxit < nancol.
Ta có thể biện luận như một số bài đã gặp ở chuyên đề đốt cháy hoặc chuyên đề anđehit từ đó tìm ra được số nguyên tử C của axit và ancol.
Ở bài này ta sẽ suy luận nhanh. Ta thấy naxit < nancol
⇒ C ¯ = 3 phải nghiêng về phía ancol hơn tức là ở gần số C của ancol hơn. Do đó ancol có 4 nguyên tử C và axit có 1 nguyên tử C.
Vậy axit là HCOOH.

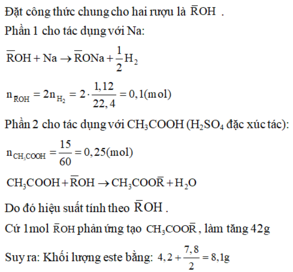

1,
- Xét phần 2:
\(n_{CH_3COOC_2H_5}=\dfrac{4,4}{88}=0,05\left(mol\right)\)
PTHH: CH3COOH + C2H5OH \(\xrightarrow[t^o]{H_2SO_{4\left(đ\right)}}\) CH3COOC2H5 + H2O
LTL: 0,5a < 0,5b (do a < b) => C2H5OH dư
Theo pthh: \(n_{CH_3COOH\left(pư\right)}=n_{CH_3COOC_2H_5}=0,05\left(mol\right)\)
Mà H = 50%
=> \(n_{CH_3COOH\left(bđ\right)}=\dfrac{0,05}{50\%}=0,1\left(mol\right)\)
Xét phần 2:
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
2CH3COOH + 2Na ---> 2CH3COONa + H2
0,1--------------------------------------------->0,05
2C2H5OH + 2Na ---> 2C2H5ONa + H2
0,4<----------------------------------------0,2
=> Trong X có: \(\left\{{}\begin{matrix}n_{CH_3COOH}=0,1.2=0,2\left(mol\right)\\n_{C_2H_5OH}=0,4.2=0,8\left(mol\right)\end{matrix}\right.\)
2, Gọi \(\left\{{}\begin{matrix}n_{CH_3COOH}=a\left(mol\right)\\n_{C_2H_5OH}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(n_{H_2O}=\dfrac{23,4}{18}=1,3\left(mol\right)\)
PTHH:
CH3COOH + 2O2 --to--> 2CO2 + 2H2O
a------------------------------------------>2a
C2H5OH + 3O2 --to--> 2CO2 + 3H2O
b-------------------------------------->3b
=> Hệ pt \(\left\{{}\begin{matrix}60a+46b=25,8\\2a+3b=1,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\left(TM\right)\)
PTHH: \(CH_3COOH+C_2H_5OH\xrightarrow[t^o]{H_2SO_{4\left(đ\right)}}CH_3COOC_2H_5+H_2O\)
LTL: 0,2 < 0,3 => Rượu dư
Theo pthh: \(n_{CH_3COOH\left(pư\right)}=n_{CH_3COOC_2H_5}=\dfrac{14,08}{88}=0,16\left(mol\right)\)
=> \(H=\dfrac{0,16}{0,2}.100\%=80\%\)