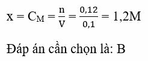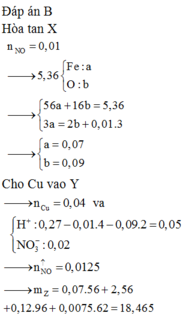Hòa tan 0.01 mol Fe2O3 và 0.02 mol Fe3O4 vào 500 ml dung dịch H2SO4 loãng 0.5 M thu được Y. Tính nồng độ mol của các chất trong Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Vì số mol của FeO bằng số mol của Fe2O3 nên ta coi hỗn hợp là Fe3O4
Ta có:
Fe3O4 +4H2SO4 → FeSO4 +Fe2(SO4)3 +4H2O
0,02 0,02
Trong 100 ml X sẽ có 0,01 mol FeSO4 nên:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
→ nKMnO4 = 0,02 mol → VKMnO4 = 0,02/0,1 = 0,2 l

a) \(n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
PTHH: 2A + H2SO4 --> A2SO4 + H2
0,8<-------------------------0,4
=> \(M_A=\dfrac{18,4}{0,8}=23\left(Na\right)\)
b)
PTHH: 2Na + H2SO4 --> Na2SO4 + H2
0,4<--------0,4<----0,4
=> \(C_{M\left(ddH_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)
\(C_{M\left(ddNa_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)

\(n_{K_2O}=\dfrac{23.5}{94}=0.25\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0.25...................0.5\)
\(C_{M_{KOH}}=\dfrac{0.5}{0.5}=1\left(M\right)\)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+H_2O\)
\(0.5............0.25............0.25\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.25\cdot98}{20\%}=122.5\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{122.5}{1.14}=107.5\left(ml\right)=0.1075\left(l\right)\)
\(C_{M_{K_2SO_4}}=\dfrac{0.25}{0.1075+0.5}=0.4\left(M\right)\)

a, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(M+H_2SO_4\rightarrow MSO_4+H_2\)
Theo PT: \(n_M=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{11,2}{0,2}=56\left(g/mol\right)\)
→ M là Fe.
b, Theo PT: \(n_{FeSO_4}=n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,2\left(mol\right)\)
⇒ nH2SO4 dư = 0,5.1 - 0,2 = 0,3 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\\C_{M_{FeSO_4}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\end{matrix}\right.\)
c, Ta có: \(n_{FeSO_4.7H_2O}=n_{FeSO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{FeSO_4.7H_2O}=0,2.278=55,6\left(g\right)\)

a) Ta có: \(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,1}{0,5}=0,2\left(M\right)=\left[Na^+\right]=\left[Cl^-\right]\)
b) Ta có: \(n_{Ba\left(OH\right)_2}=\dfrac{34,2}{171}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[Ba^{2+}\right]=0,4\left(M\right)\\\left[OH^-\right]=0,8\left(M\right)\end{matrix}\right.\)
c) Ta có: \(n_{H_2SO_4}=0,025\cdot2=0,05\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,05}{0,125+0,025}\approx0,33\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[H^+\right]=0,66\left(M\right)\\\left[SO_4^{2-}\right]=0,33\left(M\right)\end{matrix}\right.\)