Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:
CHÚC MỪNG
Bạn đã nhận được sao học tập

Chú ý:
Thành tích của bạn sẽ được cập nhật trên bảng xếp hạng sau 1 giờ!
Lý thuyết SVIP
00:00
A. Kiến thức cần nắm vững
1. Tốc độ phản ứng
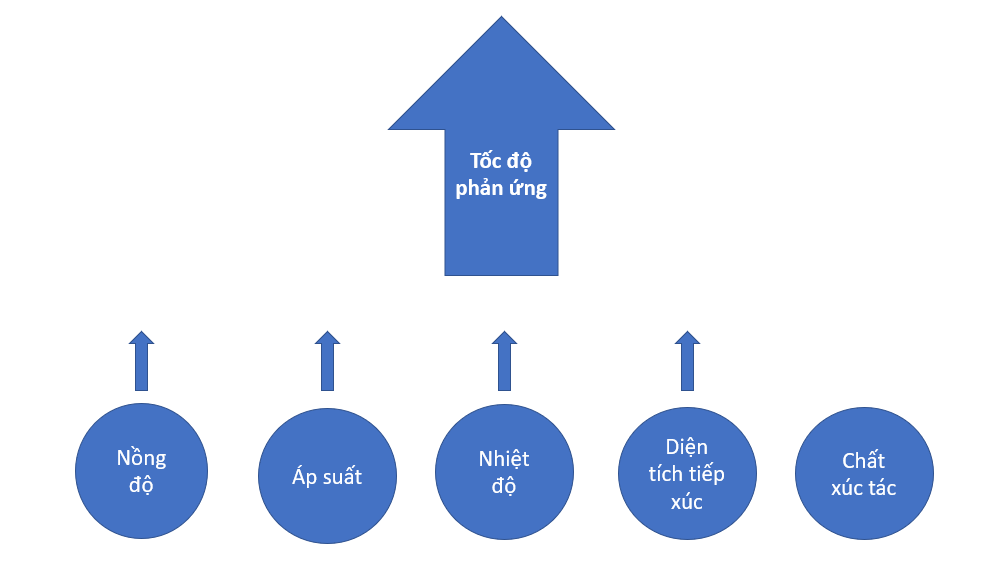
2. Cân bằng hóa học
Là trạng thái của phản ứng thuận nghịch \(V_t=V_n\) 
 .
.
Cân bằng động.
Chuyển dịch theo chiều làm giảm ảnh hưởng của tác động bên ngoài.
3. Sự chuyển dịch cân bằng
Là sự chuyển dịch từ trạng thái cân bằng này sang trạng thái cân bằng khác do tác động của các yếu tố bên ngoài lên cân bằng.
| Nồng độ (trừ chất rắn) | tăng \(C_A\) | Chiều chuyển dịch | giảm \(C_A\)   |
giảm \(C_A\)   | tăng \(C_A\)  | ||
| Áp suất | tăng | giảm số phân tử khí | |
| giảm | tăng số phân tử khí | ||
| Nhiệt độ | tăng | thu nhiệt   | |
| giảm | tỏa nhiệt  |
@98384998423@@98384999133@@98385000902@
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
OLMc◯2022

Bạn có thể đánh giá bài học này ở đây