Ngâm hỗn hợp các kim loại Al, Cu, Fe trong mỗi dung dịch sau : Dung dịch FeSO 4 (dư). Viết các phương trình hoá học. Kim loại nào thu được trong mỗi trường hợp ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Kim loại Ag thu được sau khi ngâm hỗn hợp các kim loại AI, Cu, Fe vào dung dịch AgNO 3 dư :
Al + 3 AgNO 3 → Al NO 3 3 + 3Ag ↓
Fe + 2 AgNO 3 → Fe NO 3 2 + 2Ag ↓
Cu + 2 AgNO 3 → Cu NO 3 2 + 2Ag ↓

- Kim loại Cu thu được sau khi ngâm hỗn hợp các kim loại Al, Cu, Fe vào dung dịch CuSO 4 dư
2Al + 3 CuSO 4 → Al 2 SO 4 3 + 3Cu ↓
Fe + CuSO 4 → FeSO 4 + Cu ↓

a)
Ở phần thứ 1, ngâm trong dung dịch HCl:
=> Kim loại không tan : Cu
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ở phần thứ 2 , ngâm trong dung dịch NaOH dư :
\(NaOH+Al+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\)
=> Kim loại không tan : Fe , Cu
b)
Ở phần 1 : kim loại có trong dung dịch : Cu
Ở phần 2 : kim loại có trong dung dịch : Fe , Cu
c)
- Để hòa tan Cu , dùng dung dịch AgNO3:
\(Cu+2AgNO_3\rightarrow Cu\left(NO\right)_3+2Ag\)
- Để hòa tan Fe , Cu , dùng dung dịch AgNO3 :
\(Fe+3AgNO_3\rightarrow Fe\left(NO_3\right)_3+3Ag\)
\(Cu+2AgNO_3\rightarrow Cu\left(NO\right)_3+2Ag\)
a)
Phần 1 : Kim loại không tan là Cu
Phân 2 : Kim loại không tan là Fe,Cu
b)
Phần 1 :
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Phần 2 :
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
c)
Dung dịch H2SO4 đặc nóng có thể hòa tan kim loại không tan ở mỗi phần
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O$
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$

a)
\(2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ b)\\ n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b =16,6(1)\\ n_{H_2} = 1,5a + b = \dfrac{11,2}{22,4} = 0,5(2)\\ (1)(2)\Rightarrow a = 0,2 ; b = 0,2\\ \Rightarrow m_{Al} = 0,2.27 = 5,4(gam)\ ;\ m_{Fe} = 0,2.56 = 11,2(gam)\)

Đáp án B
Al, Cu, Fe hoạt động mạnh hơn Ag đẩy được Ag ra khỏi dung dịch A g N O 3 .
Do AgNO3 dư nên Al, Cu, Fe tan hết. Chỉ thu được Ag

Phương trình hoá học của phản ứng :
Ag không tác dụng với oxi, không tác dụng với dung dịch HCl nên 2,7 garn chất rắn không tan là Ag.
Hỗn hợp kim loại với oxi.
4Al + 3 O 2 → 2 Al 2 O 3
3Fe + 2 O 2 → Fe 3 O 4
2Cu + O 2 → 2CuO
Hỗn hợp chất rắn Y với dung dịch HCl
Al 2 O 3 + 6HCl → 2Al Cl 3 + 3 H 2 O
Fe 3 O 4 + 8HCl → Fe Cl 2 + 2Fe Cl 3 + 4 H 2 O
CuO + 2HCl → Cu Cl 2 + H 2 O

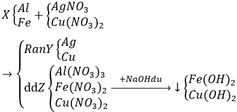
Pt:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓
2Al + 3Cu(NO3)2 → 2Al(NO3)2 + 3Cu↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3

a, PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,15.65=9,75\left(g\right)\)
\(\Rightarrow m_{Cu}=m_{hh}-m_{Zn}=21-9,75=11,25\left(g\right)\)
Bạn tham khảo nhé!
Kim loại Fe và Cu thu được sau khi ngâm hỗn hợp các kim loại AI, Cu, Fe vào dung dịch FeSO 4 dư :
2Al + 3 FeSO 4 → Al 2 SO 4 3 + 3Fe ↓