Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

200ml = 0,2l
\(n_{HCl}=2.0,2=0,4\left(mol\right)\)
Pt : \(MnO_2+4HCl_{đặc}\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O|\)
1 4 1 1 2
0,1 0,4
\(n_{MnO2}=\dfrac{0,4.1}{4}=0,1\left(mol\right)\)
⇒ \(m_{MnO2}=0,1.87=8.7\left(g\right)\)
Chúc bạn học tốt

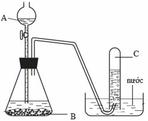
(a) Từ hình ảnh bộ dụng cụ ta thấy đây là bộ dụng cụ để điều chế các khí không tác dụng được với nước, và không tan hoặc rất ít tan trong nước
=> khí C có thể điều chế được là các khí: H2, C2H2, SO2
Cl2 và HCl không điều chế được vì tan trong nước
CO không điều chế được bằng bộ dụng cụ này trong phòng thí nghiệm.
(b)
Điều chế: H2 ; A có thể là HCl hoặc H2SO4 loãng ; B là có thể là kim loại Zn, Fe…
2HCl + Zn → ZnCl2 + H2↑
Điều chế: C2H2; A là H2O ; B là CaC2 rắn
2H2O + CaC2 → Ca(OH)2 + C2H2↑
Điều chế: SO2 ; A là HCl ; B là Na2SO3 rắn
2HCl + Na2SO3 → 2NaCl + SO2↑ + H2O

Để tránh Cl2 thoát ra ngoài không khí, người ta tẩm NaOH vào (6). Vì Cl2 có phản ứng với NaOH do đó bị giữ lại
PTPƯ
![]()
Đáp án: B

a)
A là Clo
B là SO2
C là H2S
D là NH3
E là CO2
PTHH: \(MnO_2+4HCl_{\left(đ\right)}\rightarrow MnCl_2+Cl_2\uparrow+2H_2O\)
\(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+SO_2\uparrow\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
\(NH_4HCO_3+2NaOH\rightarrow Na_2CO_3+NH_3\uparrow+2H_2O\)
\(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+CO_2\uparrow\)
b)
\(4Cl_2+H_2S+4H_2O\rightarrow H_2SO_4+8HCl\)
\(Cl_2+SO_2+2H_2O\rightarrow2HCl+H_2SO_4\)
\(SO_2+2H_2S\rightarrow3S\downarrow+2H_2O\)
\(Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
\(CO_2+2NaOH_{\left(dư\right)}\rightarrow Na_2CO_3+H_2O\)

\(\left(1\right)3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(\left(2\right)Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(\left(3\right)2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(\left(4\right)Al+NaOH+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\)
Dễ thấy thí nghiệm `(2),(4)` sinh ra `H_2` nên chọn `B`
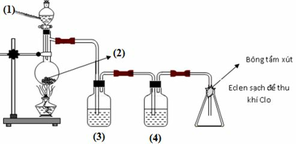
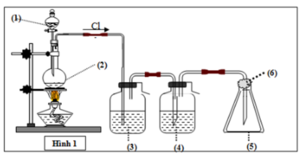
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là HCl đặc