
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right);n_{H_2SO_4}=0,1.2,5=0,25\left(mol\right)\)
PTHH: Zn + H2SO4 → ZnSO4 + H2
Mol: 0,2 0,2 0,2 0,2
Ta có: \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\) ⇒ Zn hết, H2SO4 dư
b) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c) \(m_{ZnSO_4}=0,2.161=32,2\left(g\right)\)
\(m_{H_2SO_4\left(dư\right)}=\left(0,25-0,2\right).98=4,9\left(g\right)\)
Bài 2 :
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
100ml = 0,1l
\(n_{H2SO4}=2,5.0,1=0,25\left(mol\right)\)
a) Pt : \(Zn+2H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,2 0,25 0,2 0,2
b) Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,25}{2}\)
⇒ Zn phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của Zn
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,25-0,2=0,05\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,05.98=4,9\left(g\right)\)
Chúc bạn học tốt


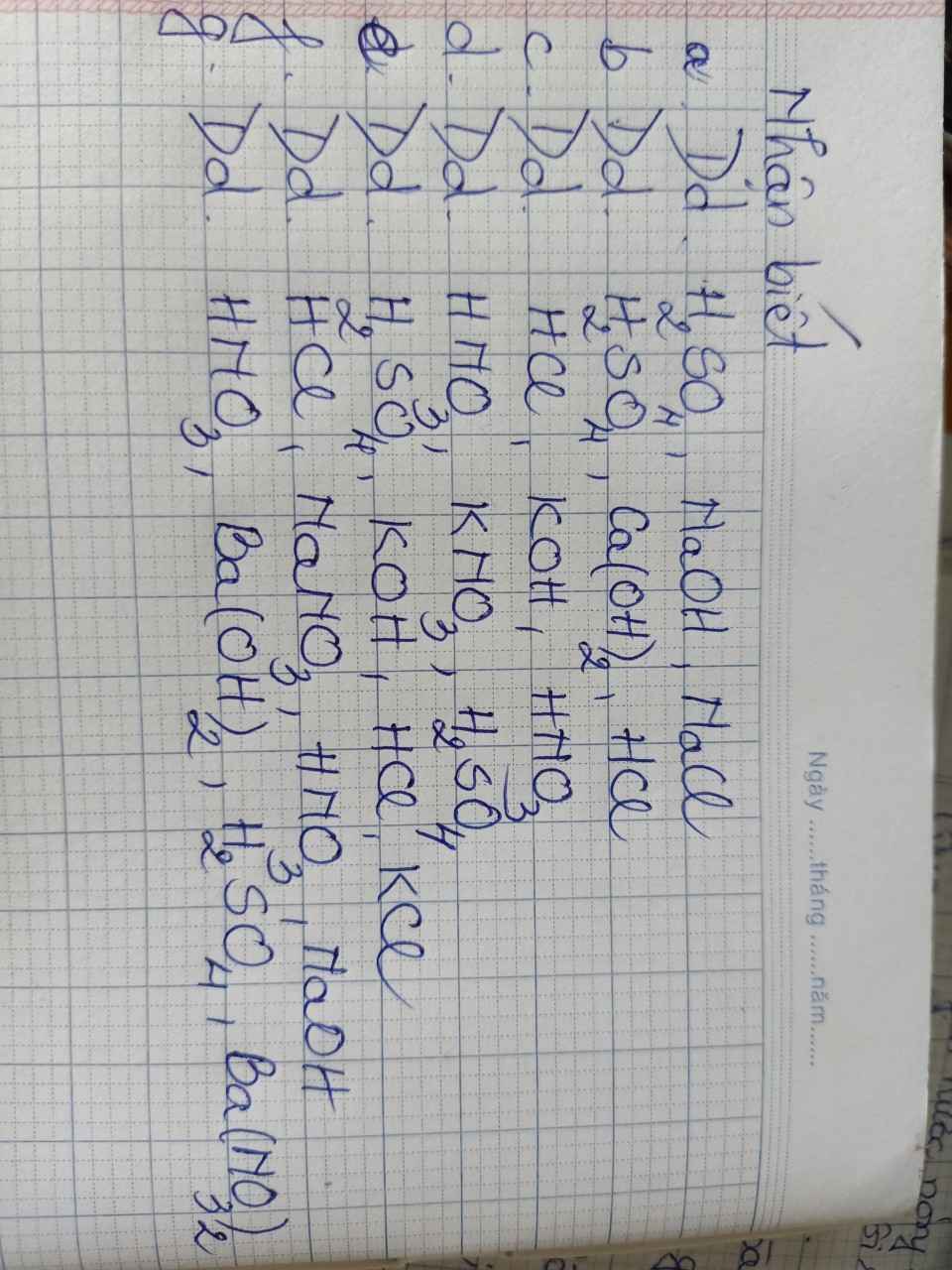
a) - Dùng quỳ tím:
+ Hóa đỏ -> dd H2SO4
+ Hóa xanh -> dd NaOH
+ Không đổi màu -> dd NaCl
b) - Dùng quỳ tím:
+ Hóa xanh -> dd Ca(OH)2
+ Hóa đỏ -> dd H2SO4, dd HCl
- Dùng dd BaCl2:
+ Có kết tủa trắng BaSO4 -> dd H2SO4
+ Không có kt trắng -> dd HCl
PTHH: H2SO4 + BaCl2 -> BaSO4 (kt trắng) + 2 HCl

a/ Gồm có nguyên tố : C và H
b/ mC= (8,8 . 12 ) / 44 = 2,4 g
mH = ( 1,8.2) / 18 = 0,2 (g)
nC : nH = (2,4:12) : (0,2:1) = 1 : 1
Công thức đơn giản nhất : CH
CTPT : (CH)n
nếu n = 1 thì MX = 13g/mol (loại)
nếu n = 2 thì MX = 26 g/mol (nhận)
Vậy CTPT của X là C2H2

Câu 4 :
100ml = 0,1l
100ml = 0,1l
\(n_{CaCl2}=0,2.0,1=0,02\left(mol\right)\)
\(n_{AgNO3}=0,1.0,1=0,01\left(mol\right)\)
a) Hiện tượng : xuất hiện kết tủa trắng
Pt : \(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl|\)
1 2 1 2
0,02 0,01 0,005 0,01
b) Lập tỉ số so sánh : \(\dfrac{0,02}{1}>\dfrac{0,01}{2}\)
⇒ CaCl2 dư , AgNO3 phản ứng hết
⇒ Tính toán dựa vào số mol của AgNO3
\(n_{AgCl}=\dfrac{0,01.2}{2}=0,01\left(mol\right)\)
⇒ \(m_{AgCl}=0,01.143,5=1,435\left(g\right)\)
c) \(n_{Ca\left(NO3\right)2}=\dfrac{0,01.1}{2}=0,005\left(mol\right)\)
\(n_{CaCl2\left(dư\right)}=0,02-\left(\dfrac{0,01}{2}\right)=0,015\left(mol\right)\)
\(V_{ddspu}=0,1+0,1=0,2\left(l\right)\)
\(C_{M_{Ca\left(NO3\right)2}}=\dfrac{0,005}{0,2}=0,025\left(M\right)\)
\(C_{M_{CaCl2\left(dư\right)}}=\dfrac{0,015}{0,2}=0,075\left(M\right)\)
Chúc bạn học tốt
Câu 5 :
\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
\(m_{ct}=\dfrac{20.100}{100}=20\left(g\right)\)
\(n_{H2SO4}=\dfrac{20}{98}=0,2\left(mol\right)\)
a) Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,02 0,2 0,02
b) Lập tỉ số so sánh : \(\dfrac{0,02}{1}< \dfrac{0,2}{1}\)
⇒ CuO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của CuO
\(n_{CuSO4}=\dfrac{0,02.1}{1}=0,02\left(mol\right)\)
⇒ \(m_{CuSO4}=0,02.160=3,2\left(g\right)\)
\(n_{H2SO4\left(dư\right)}=0,2-\left(0,02.1\right)=0,18\left(mol\right)\)
⇒ \(m_{H2SO4\left(dư\right)}=0,18.98=17,64\left(g\right)\)
\(m_{ddspu}=1,6+100=101,6\left(g\right)\)
\(C_{CuSO4}=\dfrac{3,2.100}{101,6}=3,15\)0/0
\(C_{ddH2SO4\left(dư\right)}=\dfrac{17,64.100}{101,6}=17,36\)0/0
Chúc bạn học tốt

\(a.Na+O_2-^{t^o}\rightarrow Na_2O\\ b.Cu+Cl_2-^{t^o}\rightarrow CuCl_2\\ c.Fe+2HCl\rightarrow FeCl_2+H_2\\ d.Fe+Cu\left(NO_3\right)_2\rightarrow Cu+Fe\left(NO_3\right)_2\)

Em ơi bạn ấy có ghi ở cap là cần giúp bài 3 thôi mà.

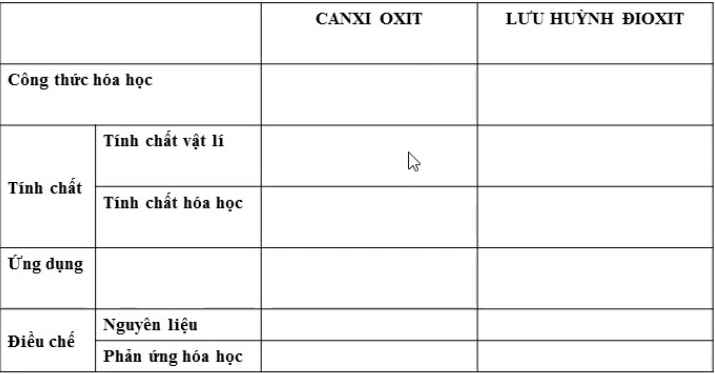






PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
a_______\(\dfrac{3}{2}\)a_________________\(\dfrac{3}{2}\)a (mol)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
b_______b_____________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+65b=11,9\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{11,9}\cdot100\%\approx45,38\%\\\%m_{Zn}=54,62\%\\n_{H_2SO_4}=0,4\left(mol\right)\Rightarrow V_{H_2SO_4}=\dfrac{0,4}{0,5}=0,8\left(l\right)\end{matrix}\right.\)