Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Na2O +H2O-->2NaOH (1)
2NaOH +CuSO4 -->Na2SO4+ Cu(OH)2 (2)
Cu(OH)2 -to-> CuO +H2O (3)
b) mNa2O=8.100/100=8(g)
=>nNa2O=8/62=0,13(mol)
theo(2) :nCu(OH)2=1/2nNaOH=0,065(mol)
theo(3):nCuO=nCu(OH)2=0,065(mol)
=>mCuO=0,065.80=5,2(g)
c) CuO +2HCl-->CuCl2+H2O (4)
theo (4) : nHCl=2nCuO=0,13(mol)
mddHCl 25%=0,13.36,5.100250,13.36,5.10025=18,98(g)

- Đánh số thứ tự các gói hóa chất, trích mỗi gói một ít hóa chất làm mẫu thử.
- Dùng HCl đặc, nóng làm thuốc thử
+ Trường hợp tạo dd màu xanh, vậy chất đầu là CuO:
C u O + 2 H C l → C u C l 2 + H 2 O
+ Trường hợp tạo dd có màu xanh rất nhạt (có thể không màu), vậy chất đầu là FeO:
F e O + 2 H C l → F e C l 2 + H 2 O
+ Trường hợp tạo ra kết tủa màu trắng, thì chất ban đầu là A g 2 O
A g 2 O + 2 H C l → 2 A g C l + H 2 O
+ Trường hợp có khí màu vàng lục thoát ra, mẫu thử là M n O 2 .
M n O 2 + 4 H C l → t 0 M n C l 2 + C l 2 + 2 H 2 O
⇒ Chọn B.

PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\downarrow\)
\(Cu\left(OH\right)_2\xrightarrow[]{t^o}CuO+H_2O\)
a) Ta có: \(n_{NaOH}=2n_{Na_2O}=2\cdot\dfrac{6,2}{62}=0,2\left(mol\right)\) \(\Rightarrow C\%_{NaOH}=\dfrac{0,2\cdot40}{6,2+193,8}\cdot100\%=4\%\)
b) Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=0,2\left(mol\right)\\n_{CuSO_4}=\dfrac{200\cdot16\%}{160}=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,2}{1}\) \(\Rightarrow\) CuSO4 còn dư, tính theo NaOH
\(\Rightarrow n_{Cu\left(OH\right)_2}=0,1\left(mol\right)=n_{CuO}\) \(\Rightarrow m_{CuO}=0,1\cdot80=8\left(g\right)\)
c) PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
Theo PTHH: \(n_{HCl}=2n_{CuO}=0,2\left(mol\right)\) \(\Rightarrow V_{ddHCl}=\dfrac{0,2}{2}=0,1\left(l\right)=100\left(ml\right)\)

Khi nhiệt phân đồng (II) hiđroxit hiện tượng quan sát được là:
A. Chất rắn từ màu đen chuyển dấn thành màu đỏ
B. Chất rắn từ màu xanh chuyển dần thành nâu đỏ
C. Chất rắn từ màu xanh chuyển dần thành màu đen
D. Chất rắn từ màu đỏ chuyển dần thành màu đen

a) mNaOH= 4%. 100= 4(g)
mCuSO4= 16%. 200= 32(g)
=> nNaOH= 4/40= 0,1(mol)
nCuSO4= 32/160= 0,2(mol)
PTHH: 2 NaOH + CuSO4 -> Cu(OH)2 + Na2SO4 (1)
Ta có: 0,1/2 < 0,2/1
=> NaOH hết, CuSO4 dư, tính theo nNaOH.
=> Kết tủa là Cu(OH)2
PTHH: (2) Cu(OH)2 -to-> CuO + H2O
n(rắn_đen)= nCuO = nCu(OH)2 (2)= nCu(OH)2 (1)= nNaOH/2= 0,1/2 0,05(mol)
=> a= m(rắn_đen)= mCuO= 0,05.80= 4(g)
b) dd A gồm dd CuSO4(dư) và dd Na2SO4
Ta có: nCuSO4(dư)= 0,2 - (0,1:2)= 0,15(mol)
=> mCuSO4(dư)= 0,15. 160= 24(g)
nNa2SO4= nNaOH/2= 0,1/2= 0,05(mol)
=> mNa2SO4= 142. 0,05= 7,1(g)
=> mddA= mddCuSO4 + mddNaOH - mCu(OH)2
<=> mddA= 200 + 100 - 0,05. 98= 295,1(g)
=> C%ddCuSO4(dư)= (24/295,1).100 \(\approx\) 8,133%
C%ddNa2SO4= (7,1/295,1).100 \(\approx\) 2,406%
c) PTHH: (3) CuO + 2 HCl -> CuCl2 + H2O
Ta có: nCuO(3)= nCuO(2)= 0,05(mol)
=> nHCl(3)= 2.0,05= 0,1(mol)
=> VddHCl= 0,1/ 2= 0,05(l)


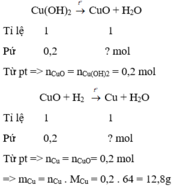
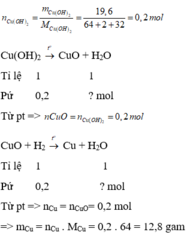
Kết tủa đen hoặc có chất bột màu đen