Có 4 dung dịch không màu bị mất nhãn sau đây: HCL, Na2SO4, NaCl, Ba(OH)2. Chỉ dùng thêm 1 hóa chất nào sau đây để phân biệt được 4 chất sau?
kẻ bảng giúp mk vs
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Trích một ít các dd làm mẫu thử
- Cho các dd tác dụng với giấy quỳ tím:
+ QT chuyển đỏ: HCl
+ QT chuyển xanh: Ba(OH)2
+ QT không chuyển màu: Na2SO4, NaCl (1)
- Cho dd ở (1) tác dụng với dd Ba(OH)2:
+ Không hiện tượng: NaCl
+ Kết tủa trắng: Na2SO4
\(Na_2SO_4+Ba\left(OH\right)_2\rightarrow2NaOH+BaSO_4\downarrow\)
Cho quỳ tím vào từng mẫu thử
+ Quỳ hóa đỏ: HCl
+ Quỳ hóa xanh: Ba(OH)2
+ Quỳ không đổi màu: NaCl, Na2SO4
Cho dung dịch Ba(OH)2 đã nhận biết được ở trên vào 2 dung dịch không làm quỳ đổi màu
+ Dung dịch nào phản ứng, xuất hiện kết tủa: Na2SO4
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaOH\)
+ Dung dịch không có hiện tượng: NaCl

Chọn A
Lấy mỗi chất 1 ít cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng.
Cho quỳ tím vào mẫu thử từng chất và quan sát, thấy:̀
- Những dung dịch làm quỳ tím đổi màu là: NaOH và Ba(O H ) 2 , (nhóm 1).
- Những dung dịch không làm quỳ tím đổi màu là: NaCl, N a 2 S O 4 (nhóm 2).
Để nhận ra từng chất trong mỗi nhóm, ta lấy một chất ở nhóm (1), lần lượt cho vào mỗi chất ở nhóm (2), nếu có kết tủa xuất hiện thì chất lấy ở nhóm (1) là Ba(O H ) 2 và chất ở nhóm (2) là N a 2 S O 4 . Từ đó nhận ra chất còn lại ở mỗi nhóm.
Phương trình phản ứng:
B a O H 2 + N a 2 S O 4 → B a S O 4 ↓ + 2 N a O H

Lấy mỗi chất ra một ít và làm thí nghiệm sau:
- Nhúng quỳ tím vào các mẫu thử:
+ quỳ chuyển đỏ: `HCl`, `H_2SO_4` (I)
+ quỳ chuyển xanh: `NaOH`, \(Ba\left(OH\right)_2\) (II)
+ quỳ không chuyển màu: \(NaCl,Na_2SO_4\) (III)
- Đem các chất ở nhóm (II) tác dụng với các chất ở nhóm (I):
+ có hiện tượng kết tủa trắng: bazo ở nhóm (II) đem tác dụng là \(Ba\left(OH\right)_2\), axit ở nhóm (I) là \(H_2SO_4\)
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
+ không hiện tượng gì: bazo đem tác dụng ở nhóm (II) là NaOH và axit ở nhóm (I) là HCl.
- Đem bazo \(Ba\left(OH\right)_2\) vừa nhận biết được tác dụng với 2 muối ở nhóm (III):
+ có hiện tượng kết tủa trắng: `Na_2SO_4`
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4\downarrow+2NaOH\)
+ không hiện tượng gì: NaCl

Chọn D
Dùng quỳ soi ra ngay HCl và HNO3, sau đó phân biệt bằng AgNO3.
KCl và KNO3 phân biệt bằng AgNO

| $HCl$ | $Ba(OH)_2$ | $Na_2CO_3$ | $MgCl_2$ | |
| $HCl$ | không hiện tượng | không hiện tượng | Khí không màu | không hiện tượng |
| $Ba(OH)_2$ | không hiện tượng | không hiện tượng | Kết tủa trắng | Kết tủa trắng |
| $Na_2CO_3$ | Khí không màu | Kết tủa trắng | không hiện tượng | Kết tủa trắng |
| $MgCl_2$ | không hiện tượng | Kết tủa trắng | Kết tủa trắng | không hiện tượng |
| Kết quả : | (1 khí) | (2 kết tủa) | (1 khí 2 kết tủa) | (2 kết tủa) |
- mẫu thử tạo 1 khí là HCl
- mẫu thử tạo 2 kết tủa là $Ba(OH)_2,MgCl_2$ - gọi là nhóm 1
- mẫu thử tạo 1 khí và 2 kết tủa là $Na_2CO_3$
Cho dung dịch $Na_2CO_3$ vào nhóm 1, lọc lấy kết tủa rồi nung đến khối lượng không đổi rồi cho vào dd $Na_2CO_3$
- mẫu thử nào tan là $Ba(OH)_2$
$Ba(OH)_2 + Na_2CO_3 \to BaCO_3 + 2NaOH$
$BaCO_3 \xrightarrow{t^o} BaO + CO_2$
$BaO + H_2O \to Ba(OH)_2$
- mẫu thử không tan là $MgCl_2$
$MgCl_2 + Na_2CO_3 \to MgCO_3 + 2NaCl$
$MgCO_3 \xrightarrow{t^o} MgO + CO_2$

Đáp án cần chọn là: C
dùng dung dịch quỳ tím ta chia thành 3 nhóm
- Nhóm (I): quỳ tím hóa đỏ : NH4Cl, H2SO4
- Nhóm (II) quỳ tím hóa xanh: NaOH, Ba(OH)2
- Nhóm (III): quỳ tím không đổi màu: NaCl, Na2SO4
- Cho lần lượt từng chất ở nhóm (II) vào từng chất ở nhóm (I)
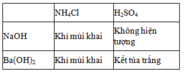
- Cho Ba(OH)2 nhận biết được vào từng chất ở nhóm (III), chất tạo kết tủa trắng là Na2SO4, chất không hiện tượng là NaCl
Lần sau nếu bn muốn ngta giả theo cách nào thì nói rõ ra nhé, chứ đăng lại mất thời gian lắm :v
- Trích một ít các dd làm mẫu thử:
\(Na_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2NaOH\)