đôt cháy hoàn toàn hỗn hợp khí gồm co và h2 cần dùng 6,72 lít khí o2.thu được 4,48 lít co2.tính phần trăm theo khối lượng và thể tích của hỗn hợp ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
2CO + O2 --to--> 2CO2
0,2<---0,1<--------0,2
2H2 + O2 --to--> 2H2O
0,4<--0,2<-------0,2
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,2+0,4}.100\%=33,33\%\\\%V_{H_2}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2CO + O2 --to--> 2CO2
0,3<--0,15<------0,3
2H2 + O2 --to--> 2H2O
0,1<--0,05
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\%n_{CO}=\dfrac{0,3}{0,3+0,1}.100\%=75\%\\\%V_{H_2}=100\%-75\%=25\%\end{matrix}\right.\)

\(n_{CO_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PTHH:
2CO + O2 --to--> 2CO2
0,2 0,1 0,2
-> nO2 = 0,3 - 0,1 = 0,2 (mol)
2H2 + O2 --to--> 2H2O
0,4 0,2
\(\rightarrow n_{hhkhí}=0,1+0,4=0,5\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,5}=40\%\\\%V_{H_2}=100\%-40\%=60\%\end{matrix}\right.\)

PTHH: \(2CO+O_2\underrightarrow{t^o}2CO_2\) (1)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\) (2)
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CO}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_{O_2\left(1\right)}=0,1\left(mol\right)\\\Sigma n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(2\right)}=0,2\left(mol\right)\) \(\Rightarrow n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow\%V_{H_2}=\dfrac{0,4}{0,4+0,2}\cdot100\%\approx66,67\%\)
\(\Rightarrow\%V_{CO}=33,33\%\)

\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(CO+\dfrac{1}{2}O_2\underrightarrow{t^o}CO_2\)
0,3 0,3
\(n_{H_2}=0,5-0,3=0,2\left(mol\right)\)
\(\%_{V_{CO}}=\dfrac{0,3.22,4.100}{11,2}=60\%\)
\(\%_{V_{H_2}}=\dfrac{0,2.22,4.100}{11,2}=40\%\)
☕T.Lam

\(n_{H_2O}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,2 0,2
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\\
\%V_{H_2}=\dfrac{4,48}{4,48+6,72}.100\%=40\%\\
\Rightarrow\%V_{O_2}=100\%-40\%=60\%\)


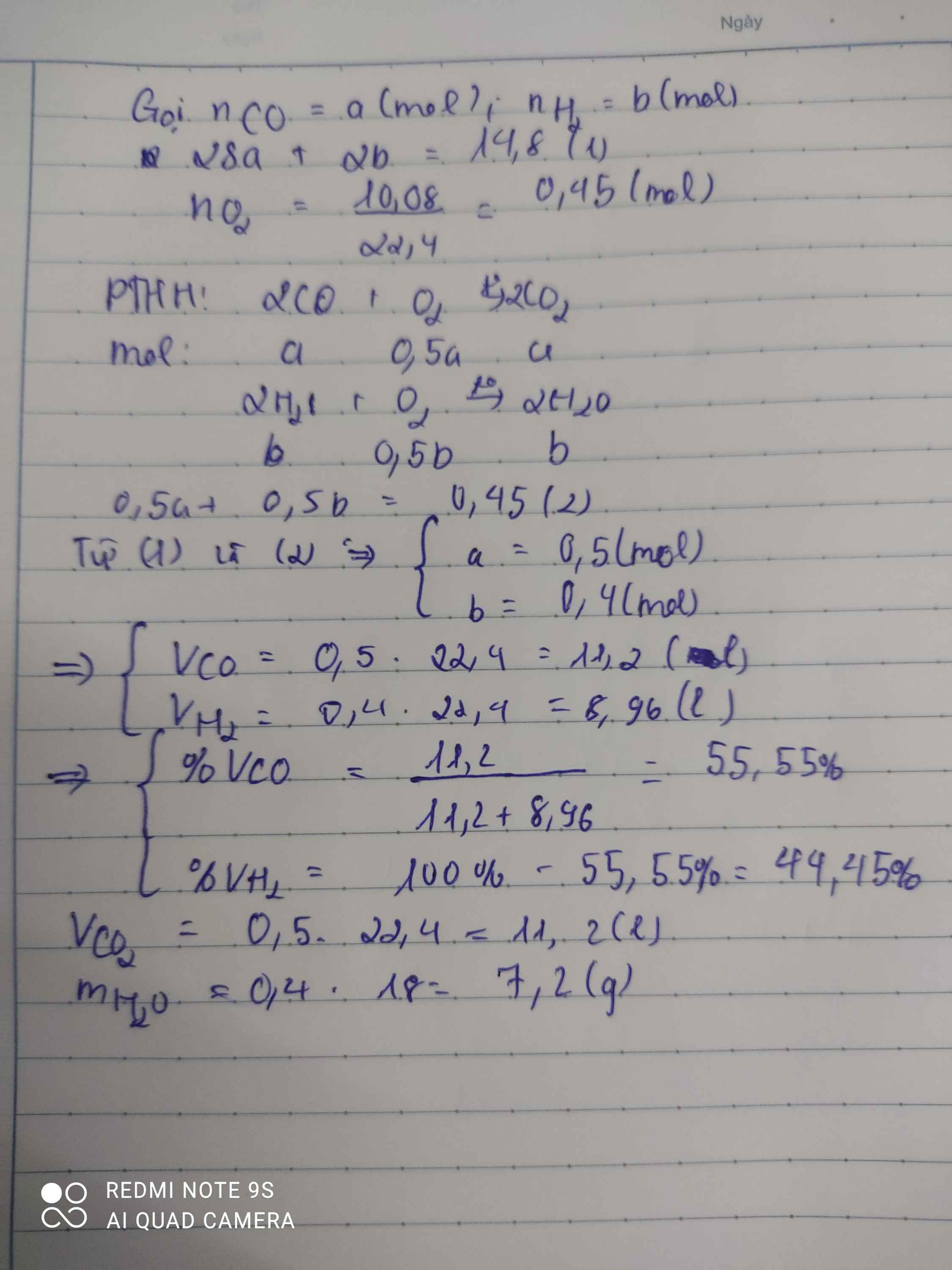
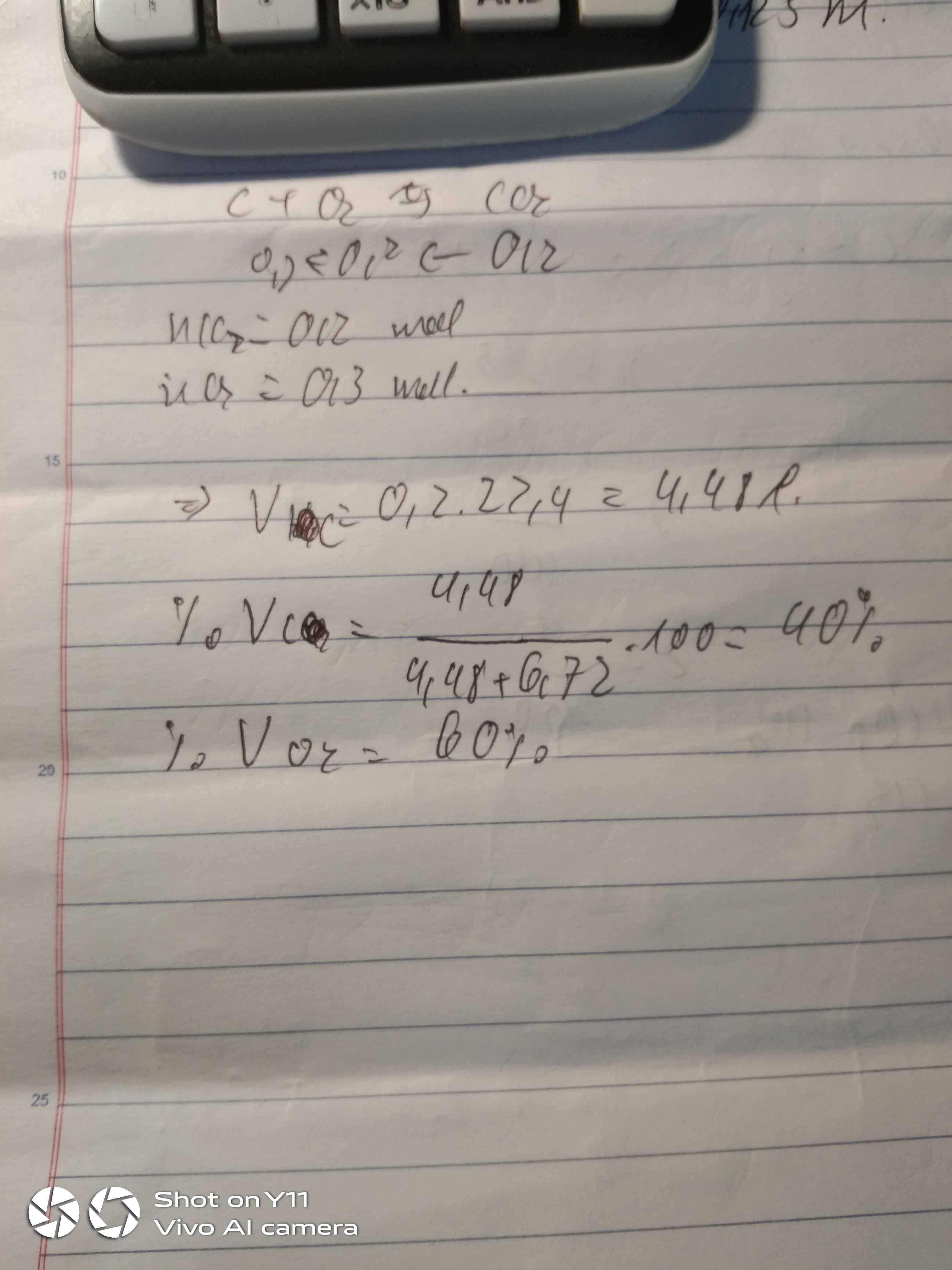
\(2CO + O_2 \xrightarrow{t^o} 2CO_2(1)\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O(2)\\ n_{CO} = n_{CO_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{O_2(1)} = \dfrac{n_{CO_2}}{2} = 0,1(mol)\\ \Rightarrow n_{H_2} = 2n_{O_2(2)} = 2.(\dfrac{6,72}{22,4}-0,1)=0,4(mol)\\ \%V_{CO} = \dfrac{0,2}{0,2+0,4}.100\% = 33,33\%\\ \%V_{H_2} = 100\% -33,33\% = 66,67\%\)
\(\%m_{CO} = \dfrac{0,2.28}{0,2.28+0,4.2}.100\% = 87,5\%\\ \%m_{H_2} = 100\% - 87,5\% = 12,5\%\)