6/ Một bình kín dung tích 8,96 lít (đktc) chứa đầy hỗn hợp X gồm N2, O2, SO2 (Tỉ lệ mol tương ứng là 2:1:1). Đốt cháy hết một lượng lưu huỳnh trong hỗn hợp X rồi đưa bình về nhiệt độ ban đầu thì thu được hỗn hợp khí Y. Biết dY/X = 1,1684. a/ Áp suất trong bình có thay đổi hay không? Vì sao? b/ Xác định phần trăm thể tích của hỗn hợp khí Y c/ Chứng minh: Khi lượng lưu huỳnh biến đổi thì 1< dY/X 1,21...
Đọc tiếp
6/ Một bình kín dung tích 8,96 lít (đktc) chứa đầy hỗn hợp X gồm N2, O2, SO2 (Tỉ lệ mol tương ứng là 2:1:1). Đốt cháy hết một lượng lưu huỳnh trong hỗn hợp X rồi đưa bình về nhiệt độ ban đầu thì thu được hỗn hợp khí Y. Biết dY/X = 1,1684. a/ Áp suất trong bình có thay đổi hay không? Vì sao? b/ Xác định phần trăm thể tích của hỗn hợp khí Y c/ Chứng minh: Khi lượng lưu huỳnh biến đổi thì 1< dY/X 1,21 các Mod Hoidap247 vào giúp với ạ


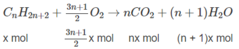
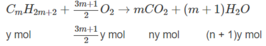
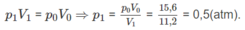
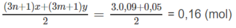
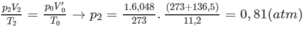
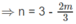
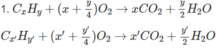



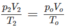
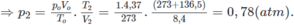
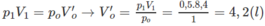
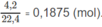
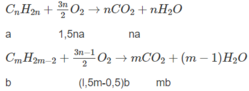

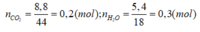
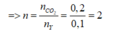
Đáp án: D
Phản ứng xảy ra:
2H2 + O2 → 2H2O.
Theo đó 12g Oxy sẽ kết hợp với 4.12/32 = 1,5g Hidro và thành 13,5 g hơi nước.
Sau phản ứng trong bình có m1 = 3,5g khí hidro và m2 = 13,5g hơi nước.
Lượng nhiệt tỏa ra từ phản ứng là:
Q = Q0.13,5/18 = 1,8.105J.
Lượng nhiệt này sẽ làm tăng nội năng của hơi nước và khí hidro.
Ta có: Q = (c1m1 + c2m2)∆T
=> Nhiệt độ khí trong bình là
T = T0 + ∆T =2589 K
Vậy áp suất trong bình là:
p = p1 + p2