Hòa tan hoàn toàn hỗn hợp gồm 0,01 mol Al; 0,05 mol Zn và 0,03 mol Fe cần vừa đủ 200ml dung dịch HCl 0,1M và H2SO4 a mol/l. Giá trị của a là?
A. 0,425
B. 0,5
C. 0,625
D. 0,75
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Hướng dẫn
A,C sai: HCl và H2SO4 loãng không hòa tan được kim loại đứng sau H trong dãy hoạt động hóa học như Cu, Ag
D sai: H2SO4 đặc nguội không hòa tan được Al, Fe (Al, Fe bị thụ động hóa trong H2SO4 đặc nguội và HNO3 đặc nguội)

Đáp án C
Hướng dẫn
Kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối của chúng
Nên chọn muối của KL yếu nhất là AgNO3

Đáp án C
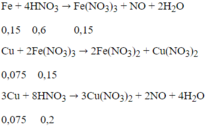
Số mol HNO3 cần dùng là: 0,6 + 0,2 = 0,8 mol
Thể tích dung dịch HNO3 1M cần dùng là:


Coi hỗn hợp Y gồm : Kim loại và Oxi
$n_O = \dfrac{2,71-2,23}{16}= 0,03(mol)$
Gọi $n_{H_2SO_4\ pư}= a(mol)$
$n_{SO_2} = \dfrac{1,008}{22,4} = 0,045(mol)$
Bảo toàn nguyên tố với H : $n_{H_2O} = n_{H_2SO_4\ pư} = a(mol)$
Bảo toàn nguyên tố với S :
$n_{SO_4(trong\ muối)} = n_{H_2SO_4} - n_{SO_2} = a - 0,045(mol)$
Bảo toàn nguyên tố với O :
$0,03 + 4a = (a - 0,045).4 + 0,045.2 + a$
$\Rightarrow a = 0,12(mol)$

mKL 1phần = 5g
TN1: td với O2
Bảo toàn kl
⇒mO2=5,32-5=0,32g
⇒mol O2=0,01 mol
⇒V=0,224l
O2+4e→2O2−
−0,01 mol⇒⇒0,04 mol
Mol e nhận=0,04 mol
P2: lượng KL vẫn thế
⇒mol e nhận và nhường ko đổi=0,04 mol
2H++2e→H2
0,04 mol⇐0,04 mol⇒0,02 mol
V'=0,02.22,4=0,448l
Mol HCl=2mol
H2=0,04 mol
⇒mHClmHCl=1,46g
Bảo toàn klg=>m=5+1,46-0,02.2=6,42g

a) Gọi số mol Fe, Mg là a, b (mol)
=> 56a + 24b = 1,04 (1)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
a--->2a-------------->a
Mg + 2HCl --> MgCl2 + H2
b---->2b------------->b
=> a + b = 0,03 (2)
(1)(2) => a = 0,01 (mol); b = 0,02 (mol)
mFe = 0,01.56 = 0,56 (g)
mMg = 0,02.24 = 0,48 (g)
b) nHCl(lý thuyết) = 2a + 2b = 0,06 (mol)
=> \(n_{HCl\left(tt\right)}=\dfrac{0,06.110}{100}=0,066\left(mol\right)\)
=> \(V_{dd.HCl\left(tt\right)}=\dfrac{0,066}{0,1}=0,66\left(l\right)\)
Đáp án A
Ta có: ne cho = ne nhận = nH+
⇒ 0,02 + 0,4a = 0,19 → a = 0,425