Hoà tan hoàn toàn kim loại M trong dd hcl 10 phần trăm vừa đủ.dd thu đc sau pư có nồng độ phần trăm của muối tạo thành là 17,15 phần trăm.Xác định kim loại M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giả sử có 1 mol RCO3
PTHH: RCO3 + 2HCl → RCl2 + CO2↑ + H2O
1 → 2 1 1 1 (mol)
Ta có mdd(sau pứ) = mRCO3+mdd(HCl)−mCO2
⟹ mdd(sau pứ) = \(\dfrac{\text{MR+60+(2.36,5.100%)}}{7,3\%-1,44}\)=MR+1016
⟹ C%(RCl2)=mRCl2mdd(sau).100%=\(\dfrac{M_{R_{ }}+71}{_{ }M_R+1016}\).100%=9,135%
⟹ MR = 24 (Mg)
Vậy công thức của muối là MgCO3.

\(a)n_{H_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ n_{Al}=a;n_{Fe}=b\\ \left\{{}\begin{matrix}1,5a+b=0,2\\27a+56b=5,5\end{matrix}\right.\\ a=0,1\\ b=0,05\\ \%_{Al}=\dfrac{0,1.27}{5,5}\cdot100=49\%\\ \%_{Fe}=100-49=51\%\\ b)n_{HCl\left(1\right)_{ }}=0,1\cdot\dfrac{6}{2}=0,3\left(mol\right)\\ n_{HCl\left(2\right)}=0,05.2=0,1\left(mol\right)\\ n_{HCl}=0,3+0,1=0,4\left(mol\right)\\ C_{M_{HCl}}=\dfrac{0.4}{0,5}=0,8M\)

Đáp án A
Gọi n là hoá trị của M; x là số mol của M
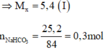
Phương trình hoá học:
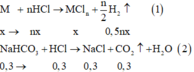
Dung dịch X thu được gồm NaCl: 0,3 mol; MCn: x mol; HCl dư

Tổ hợp (I) và (II) ta được:
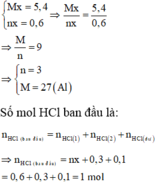
Số mol các khí thu được theo (1), (2) là:
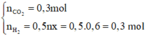
Nồng độ phần trăm của NaCl trong dung dịch X là:
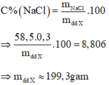
Mặt khác, ta có:
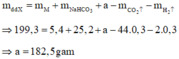
Nồng độ phần trăm dung dịch HCl ban đầu là:
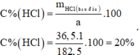

\(a)n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\\ n_{Fe}=a;n_{Al}=b\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow\left\{{}\begin{matrix}56a+27b=11\\a+1,5b=0,4\end{matrix}\right.\\ \Rightarrow a=0,1;b=0,2\)
\(\%m_{Fe}=\dfrac{0,1.56}{11}\cdot100=50,91\%\\ \%m_{Al}=100-50,91=49,09\%\)
\(b)Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,2 0,1 0,1
\(2Al+6HCl\rightarrow2AlCl_2+3H_2\)
0,2 0,6 0,2 0,3
\(m_{HCl}=\dfrac{\left(0,2+0,6\right).36,5}{9,125}\cdot100=320g\)
\(c)m_{dd}=320+11-0,1.2-0,3.2=308,2g\)
\(C_{\%FeCl_2}=\dfrac{0,1.127}{308,2}\cdot100=4,12\%\\ C_{\%AlCl_3}=\dfrac{0,2.133,5}{308,2}\cdot100=8,66\%\)

\(m_{dd.HCl}=1,08.150=162\left(g\right)\)
\(n_{CO_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
\(RCO_3+2HCl\rightarrow RCl_2+H_2O+CO_2\)
0,15<----------------0,15<-----------0,15
Có: \(R+60=\dfrac{12,6}{0,15}\Rightarrow R=24\left(g/mol\right)\)
a. Kim loại R là Magie (Mg)
b. \(C\%_{MgCl_2}=\dfrac{0,15.95.100\%}{12,6+162-0,15.44}=8,48\%\)
c. \(n_{AgCl}=\dfrac{53,8125}{143,5}=0,375\left(mol\right)\)
\(MgCl_2+2AgNO_3\rightarrow2AgCl+Mg\left(NO_3\right)_2\)
0,15-------------------->0,3
Vì \(n_{AgCl}=0,3\left(mol\right)< 0,375\left(mol\right)_{theo.đề}\) \(\Rightarrow\) HCl dư
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\)
0,075<------------0,075
\(CM_{HCl.đem.dùng}=\dfrac{0,075}{0,15}=0,5M\)

nH2=0,15 mol
2Al+3H2SO4=>Al2(SO4)3+3H2
0,1 mol<= 0,15 mol
mAl=0,1.27=2,7g
nAl2(SO4)3=0,05 mol
=>mAl2(SO4)3=342.0,05=17,1g
nH2SO4=0,15 mol=>mH2SO4=14,7
mdd H2SO4=14,7/10%=147g
mdd sau pứ=2,7+147-0,15.2=149,4g
C%dd Al2(SO4)3=17,1/149,4.100%=11,45%

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ a,Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=0,1(mol);n_{HCl}=0,2(mol)\\ \Rightarrow m_{Fe}=0,1.56=5,6(g)\\ C_{M_{HCl}}=\dfrac{0,2}{0,25}=0,8M\\ b,m_{dd_{HCl}}=250.1,12=280(g)\\ n_{FeCl_2}=0,1(mol)\\ \Rightarrow C\%_{FeCl_2}=\dfrac{0,1.127}{5,6+280-0,1.2}.100\%=4,45\%\)
