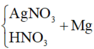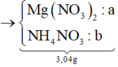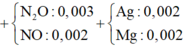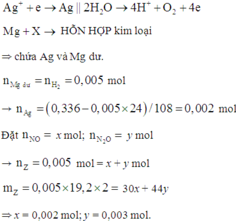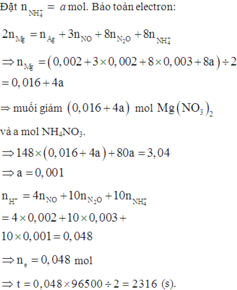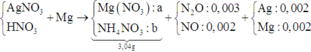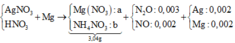Câu 1: Cho 3,04 gam hỗn hợp gồm kim loại Fe và R có hóa trị II, tác dụng hết với dung dịch HCl thu được 1,344 lít khí ở đktc và dung dịch X. Cho 3,04 gam kim loại R vào 98gam dung dịch H2SO4 8% thấy H2SO4 còn dư. Kim loại R là
A. Mg B. Ca C. Zn D. Ba
Câu 2: Hòa tan hoang toàn 6,9 gam muối cacbonat của kim loại hóa trị I (không đổi), cần dùng vừa đủ 200 ml dung dịch H2SO4 có khối lượng riêng 1,2 (g/ml). Thu được 244, 7 gam dung dịch Y. Nồng độ phần trăm (C%) của chất tan trong dung dịch Y là:
A. 3,55 (%). B. 3,19 (%). C. 1,15(%). D. 3,0 (%).