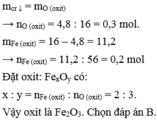Khử hoàn toàn 16g oxit Fe bằng CO ở nhiệt độ cao. Sau PU thấy khổi lượng của chất rắn giảm 4,8g.
a/ T ìm CTPT của oxit Fe
b/ Khí sinh ra dẫn qua bình đựng dd NAOH dư. Khối lượng của bình tăng hay giảm?
c/ Tính thể tích của CO đã dùng (đktc). Biết CO lấy dư 20% so với lý thuyết