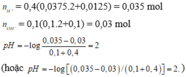1.Trộn 100ml dd HCl 0,1M và HNO3 0,1M vào 100ml dd NaOH 0,1M và Ca(OH)2 0,1M. Tính pH dd?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt V (l) là thể tích dung dịch bazo cần tìm.
Ta có:
Mà
+)
(vì có 2 nhóm trong dd ).
Ta có phương trình ion thu gọn sau:
Theo PTHH:

*dd A : n( H+) / HCI +n ( H+)/ HNO3
= ( 0,1* 0,2 ) + ( 0,1 *0,1 )= 0,02 +0,01 = 0,03 mol
______ n ( CI-) = 0,1*0,2 = 0,02 mol
______n ( NO3) = 0,1*0,1 = 0,01 mol
* BA (OH) 2 vào trung hòa thực chất là phản ứng tạo nước
( OH- )+ (H+)----------> H2O
0,03<------ 0,03
Vậy lượng ( OH-) cần để trung hào 300ml dd A là 0,03 mol ( HCI 200ml + HNO3 100ml =300ml )
=> Để trung hòa 100ml dd A cần n (OH-) = 1/3 số mol cần trung hào 300ml = 0,03 /3 = 0,01mol
=> nBa ( OH )2 = 1/2 n ( OH- )= 0,01/2 = 0,005 mol
=> VBa (OH) 2 = n / Cm = 0,005 / 0,02 = 0,25 lít = 250ml

\(n_{H^+}=0.3\cdot0.1\cdot2+0.3\cdot0.15=0.105\left(mol\right)\)
\(n_{OH^-}=0.001V\cdot0.3+0.001V\cdot2\cdot0.1=0.0032V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.105.......0.105\)
\(n_{OH^-\left(dư\right)}=0.0032V-0.105\left(mol\right)\)
\(\left[OH^-\right]=\dfrac{0.0032V-0.105}{0.3+0.001V}\left(M\right)\)
\(pH=14+log\left[OH^-\right]=12\)
\(\Leftrightarrow log\left[OH^-\right]=-2\)
\(\Leftrightarrow log\left[\dfrac{0.0032V-0.105}{0.3+0.001V}\right]=-2\)
\(\Leftrightarrow V=33.85\left(ml\right)\)
nH+=0,3.0,1.2+0,3.0,15=0,105 mol
nOH- ban đầu =0,3V + 0,1.2V=0,5V mol
Sau phản ứng thu được dung dịch có pH=12
⇒OH- dư ⇒ pOH=2
⇒ [OH- ] dư = 0,01 M
nOH- dư = 0,01(0,3+V)=0,003+0,01V (mol)
nOH- phản ứng=nOH- ban đầu - nOH- dư
= 0,5V - 0,003 - 0,01V
= 0,49V - 0,003 (mol )
H+ + OH- → H2O
0,105 → 0,105
nOH- phản ứng = nH+
⇒0,49V - 0,003 =0,105
⇒ V≃0,22 lít=200ml