Trong một bình người ta trộn hai khí SO2 và SO3.Khi phân tích thì thấy có 2,4 gam lưu huỳnh và 2,8 gam oxi.Tính tỉ số mol SO2 và số mol SO3 trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) nS = 2,4/32= 0,075(mol)
nO2= 2,8/32=0,0875(mol)
PTHH: S+ O2 -to-> SO2 (1)
Ta có: 0,075/1 < 0,0875/1
=> S hết, O2 dư => Tính theo nS
-> nO2(p.ứ)=nSO2=nS=0,075(mol)
=> nO2(dư)=0,0875 - 0,075=0,0125(mol)
2 SO2 + O2 \(⇌\left(t^o,xt\right)\) 2 SO3 (2)
Ta có: nSO2(2)= nSO3= nO2(dư)=0,0125(mol)
=> nSO2(còn)= 0,075 - 0,0125= 0,0625(mol)
Tỉ số mol SO2 và SO3 trong hỗn hợp trên:
\(\dfrac{n_{SO2}}{n_{SO3}}=\dfrac{0,0625}{0,0125}=5\)

\(n_S=\dfrac{0,4}{32}=0,0125\left(mol\right);n_O=\dfrac{2,8}{16}=0,175\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{SO_2}=a\left(mol\right)\\n_{SO_3}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_S=n_{SO_2}+n_{SO_3}=a+b=0,0125\\n_O=2n_{SO_2}+3n_{SO_3}=2a+3b=0,175\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=-0,1375\left(mol\right)\\b=0,15\left(mol\right)\end{matrix}\right.\)
Đề sai à bạn?
dạ em ghi y chang đề thầy cho, mà anh/chị thấy đề vô lý ở chỗ nào ạ? có khi em chép sai cũng nên

Trong hỗn hợp Y: Đặt
![]()
Vì SO2 dư nên kết tủa Z gồm BaSO4 và BaSO3
Ta có:
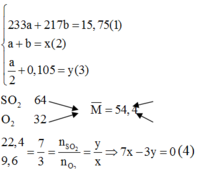



*Theo đề bài
nS= 2,4/32=0,075(mol)
nO = 2,8/32=0,175(mol)
* Ta có :
Tổng số nguyên tử S ở SO2 và SO3 lần lượt là 1,1 => tỉ lệ số mol : 1:1 = 0,0375:0,0375
tổng____________O____________-________2:3> tỉ lệ số mol 2:3=0,07:0,105
\(\Sigma_{SO2}=0,07+0,0375=0,1075\)(mol)
\(\Sigma_{SO3}=0,105+\)0,0375=0,1425(mol)
=>tỉ lệ \(\dfrac{SO_2}{SO_3}=\dfrac{0,1075}{0,1425}=\dfrac{43}{57}\)
P/S : có thể là sai , tôi đoán 70% sai
Hoang Thiên Di số mol của O2 là 2,8/32=0,0875 mol