Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Axit: là những chất phân li trong nước ra ion H+
Ví dụ:
HCl → H+ + Cl-
H2S ⇌ 2H+ + S2-
- Axit một nấc: là những axit chỉ phân li một nấc ra ion H+ thí dụ như HCl, HBr…
HCl → H+ + Cl-
- Axit nhiều nấc là những axit phân li nhiều lần ra H+
Ví dụ:
| H2S là axit hai nấc | H2S ⇔ H+ + HS- HS- ⇌ H+ + S2- |
| H3PO4 là axit ba nấc | H3PO4 ⇌ H+ + H2PO4- H2PO4- ⇌ H+ + HPO42- HPO42- ⇌ H+ + PO43- |

Viết phương trình điện li của các chất sau đây trong dung dịch :
1. Axit mạnh H2SeO4 (nấc thứ nhất điện li mạnh)
\(H_2SeO_4\rightarrow H^++HSeO_4^-\)
\(HSeO_4^-\leftrightarrow H^++SeO_4^{2-}\)
2. Axit yếu 3 nấc H3PO4
\(H_3PO_4\leftrightarrow H^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
3. Hiđroxit lưỡng tính Pb(OH)2
\(Pb\left(OH\right)_2\leftrightarrow Pb^{2+}+2OH^-\)
\(Pb\left(OH\right)_2\leftrightarrow PbO_2^{2-}+2H^+\)
4. Na2HPO4
\(Na_2HPO_4\leftrightarrow2Na^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
5. NaH2PO4
\(NaH_2PO_4\leftrightarrow Na^++H_2PO_4^-\)
\(H_2PO_4^-\leftrightarrow H^++HPO_4^{2-}\)
\(HPO_4^{2-}\leftrightarrow H^++PO_4^{3-}\)
6. Axit mạnh HMnO4
\(HMnO_4\rightarrow H^++MnO_4^-\)
7. Bazơ mạnh RbOH
\(RbOH\rightarrow Rb^++OH^-\)

Gọi số mol của axit axetic và axit fomic lần lượt là x và y (mol)
Phương trình hoá học ở dạng phân tử:
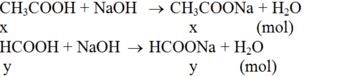
Phương trình hoá học ở dạng ion:
CH3COOH + OH- → CH3COO- + H2O
HCOOH + OH- → HCOO- + H2O

- Sản phẩm của phản ứng giữa dung dịch axit và hiđroxit bazơ là muối và nước (H2O), mà nước là chất điện li yếu.
Ví dụ: Mg(OH)2 + 2HCl → MgCl2 + 2H2O
- Sản phẩm của phản ứng giữa muối cacbonat và dung dịch axit là muối mới, và axit cacbonic (H2CO3) rất yếu, dễ dàng bị phân huỷ thành nước (H2O và khí cacbonic (CO2) Vậy sản phẩm cuối cùng sau phản ứng có chất dễ bay hơi (CO2) và chất điện li yếu (H2O).
Ví dụ: CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
- Theo điều kiện của phản ứng trao đổi thì phản ứng trên xảy ra được.

Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
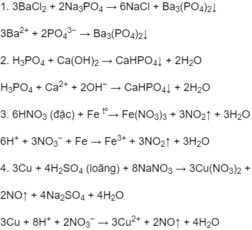

\(\text{Axit: HCl, H2SO4, HNO3,.... Vì những chất này là axit mạnh}\\ \text{Bazo : NaOH, Ba(OH)2, KOH,, Ca(OH)2. Vì những chất này là bazo mạnh, đi với nhóm OH ggòm: K, Ca, Ba,Na}\\ \text{Muối: NaCl, MgCl_2, ,K2CO3, KCl.... Vì những chất này là muối tan}\)

Theo thuyết A-rê-ni-ut thì:
– Axit là chất khi tan trong nước phân li ra cation H+
Ví dụ: HCl → H+ + Cl–
– Bazơ là chất khi tan trong nước phân li ra anion OH–
Ví dụ : NaOH → Na+ + OH–
– Hiđroxit lưỡng tính là hiđroxit khi tan trong nước vừa có thể phân li như axit, vừa có thể phân li như bazơ.
Zn(OH)2 ⇔ Zn2+ +20H– ; Zn(OH)2 ⇔ ZnO2-2 + 2H+
2. Những axit mà tan trong nước phân li nhiều nấc ra ion H+ gọi là các axit nhiều nấc.
Ví dụ : H2SO4, H3PO4….
Những bazơ khi tan trong nước phân li nhiều nấc ra ion OH– gọi là các bazơ nhiều nấc. Ví dụ : Mg(OH)2, Ca(OH)2,….
3. Muối là hợp chất, khi tan trong nước phân li ra cation kim loại (hoặc cation NH4+) và anion gốc axit. Ví dụ : Na2CO3 → 2Na+ + CO32-
Muối trung hòa là muối mà anion gốc axit không có khả năng phân li ra ion H+. Muối axit là muối mà anion gốc axit có khá năng phân li ra ion H+.
Sự điện li cùa muối trong nước tạo cation kim loại (hoặc NH4+ , ion phức) và anion gốc axil.