Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Al sẽ phản ứng được với dung dịch muối của kim loại yếu hơn Al
=> kim loại yếu hơn Al là Cu
P T H H : 2 A l + 3 C u S O 4 → 3 C u + A l 2 S O 4 3

1) Bằng phương pháp hóa học hãy trình bày cách nhận biết các dung dịch không
màu sau: HNO3, KOH, H2SO4, KCl
Trích mỗi lọ 1 ít làm mẫu thử
Cho quỳ tím vào mẫu thử
+ Quỳ hóa xanh : KOH
+ Quỳ hóa đỏ : HCl, H2SO4
+ Không đổi màu : KCl
Cho dung dịch BaCl2 vào 2 mẫu làm quỳ hóa đỏ
+ Kết tủa: H2SO4
H2SO4 + BaCl2 ---------> BaSO4 + 2HCl
+ Không hiện tượng : HCl
2) Hiện tượng gì xảy ra khi cho axit H2SO4 vào ống nghiệm chứa bột Al màu
trắng xám.Viết phương trình hóa học xảy ra.
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
Hiện tượng: Chất rắn màu trắng bạc của nhôm (Al) tan dần trong dung dịch, xuất hiện khí hidro (H2) làm sủi bọt khí.

(a) CO2 + NaOH → NaHCO3
Dung dịch sau pứ chỉ có NaHCO3
(b) 2NaOH + Ca(HCO3)2 → Na2CO3 + CaCO3 + H2O
Dung dịch sau pứ: (Na2CO3; NaOH dư)
(c) Ba(HCO3)2 + H2SO4 → BaSO4 + 2CO2 + 2H2O
Dung dịch sau pứ: Ba(HCO3)2 dư
(d) Mg + CuSO4 → MgSO4 + Cu
Dung dịch sau pứ: (MgSO4; CuSO4 dư)
(e) Na + H2O → NaOH + ½ H2
NaOH + CH3COOH → CH3COONa + H2O
Dung dịch sau pứ: (NaOH dư; CH3COONa)
(f) Dung dịch sau pứ: (C6H6; Br2/H2O)

- Trích mẫu thử, cho quỳ tím vào các mẫu thử:
+ Quỳ hóa đỏ: \(Fe_2(SO_4)_3\)
+ Quỳ hóa xanh: \(Na_2CO_3\)
+ Quỳ ko đổi màu: \(BaCl_2,Na_2SO_4(1)\)
- Cho \(Ba(OH)_2\) vào nhóm \((1)\), xuất hiện kết tủa là \(Na_2SO_4\), còn lại là \(BaCl_2\)
\(PTHH:Ba(OH)_2+Na_2SO_4\to BaSO_4\downarrow+2NaOH\)

Xử lí bài tập nhận biết, ta chỉ cần thử 1 trong 5 hóa chất hữu dụng sau: Ba(OH)2, H2SO4, AgNO3, Quì tím, HCl. Trích mỗi ống nghiệm ra làm nhiều mẫu thử, đánh số thứ tự để thuận tiện đối chiếu kết quả thực nghiệm.
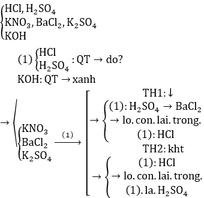
Lấy ngẫu nhiên 1 lọ thuộc nhóm (1) (nhóm axit) để nhận biết nhóm (2)
Dùng BaCl2 nhận biết KNO3 và K2SO4
Pt: BaCl2 + H2SO4 → 2HCl + BaSO4↓
BaCl2 + K2SO4 → 2KCl + BaSO4↓

1) Kẽm tan dần, xuất hiện khí không màu không mùi
$Zn + 2HCl \to ZnCl_2 + H_2$
2) Xuất hiện kết tủa màu trắng
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
3) Xuất hiện kết tủa màu trắng
$BaCl_2 + Na_2CO_3 \to BaCO_3 + 2NaCl$
4) Ban đầu giấy quỳ tím màu xanh sau đó chuyển không màu và chuyển màu đỏ nếu cho HCl dư
$NaOH + HCl \to NaCl + h_2O$
5) Đinh tan dần, có chất rắn màu nâu đỏ bám vào đinh, dd chuyển dần từ xanh lam sang không màu
$Fe + CuSO_4 \to FeSO_4 + Cu$
6) Xuất hiện kết tủa màu xanh lam, nung kết tủa thì được chất rắn màu đen
$CuSO_4 + 2NaOH \to Cu(OH)_2 + Na_2SO_4$
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$

- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ hóa đỏ: HCl
+ Quỳ không đổi màu: NaCl, Na2SO4 (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: Na2SO4
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)
+ Không hiện tượng: NaCl
- Dán nhãn.
BaO sẽ tan vào nước trong dd tạo Ba(OH)2
Chỉ có đáp án A sai